锋芒初露!药企13款创新药亮眼,2大爆品独家过评,猛攻吸入剂,挑战$45亿明星药
来源:米内网时间:2020-10-23分类:医药行业新闻
手机访问
扫一扫,发送至微信
近日,海思科产品线动态连连:培哚普利叔丁胺片首家过评,HSK3486乳状注射液新适应获准开展III期临床,FTP-198片申报临床......作为创新药新锐,海思科近几年来不断加大研发投入,2020年H1研发投入占营收比重突破20%。目前公司有4个品种过评(2个独家),在审品种中,9个注射剂提交一致性评价补充申请(5个年销超10亿),10个品种以新分类报产(4个未有首仿);13款创新药在研,其中6款已开展临床,首个1类新药获批在即。
精彩内容
近日,海思科产品线动态连连:培哚普利叔丁胺片首家过评,HSK3486乳状注射液新适应获准开展III期临床,FTP-198片申报临床......作为创新药新锐,海思科近几年来不断加大研发投入,2020年H1研发投入占营收比重突破20%。目前公司有4个品种过评(2个独家),在审品种中,9个注射剂提交一致性评价补充申请(5个年销超10亿),10个品种以新分类报产(4个未有首仿);13款创新药在研,其中6款已开展临床,首个1类新药获批在即。
研发占比突破20%,产品管线动态连连
海思科于2012年成功登陆深交所,现有产品主要为注射剂,且绝大部分为国内首家或独家仿制,首仿率超过34%,在肠外营养、肝病、抗感染等细分领域占据重要地位。
图:2016-2020年同期海思科研发投入情况(单位:亿元)

来源:上市公司公告
从2018年开始,海思科在创新药的研发投入开始超过仿制药。在2020年疫情影响下,海思科仍持续加大研发力度,上半年研发投入3.04亿元,比去年同期增长32.82%,研发投入占营业收入比重为20.91%,超过恒瑞(16.49%)、复星(12.06%)、中国生物制药(12.18%)、石药(11.54%)等国内头部企业。
截至2020年上半年,海思科在研制剂项目79个,包括仿制药59个,创新药13个,特殊医学用途配方食品6个,医疗器械1个;涵盖4大治疗领域,其中消化系统及代谢领域35个、神经系统领域8个、呼吸系统领域7个、心脑血管系统领域7个、其他领域22个。
据海思科年报数据,未来公司争取实现每年1-2个创新药(含新适应证)上市销售;每年2-3个创新药申报IND;每年2-3个外部合作项目有效落地;研发投入占营收比重不低于12%。
表1:2020年至今海思科公告的部分产品动态
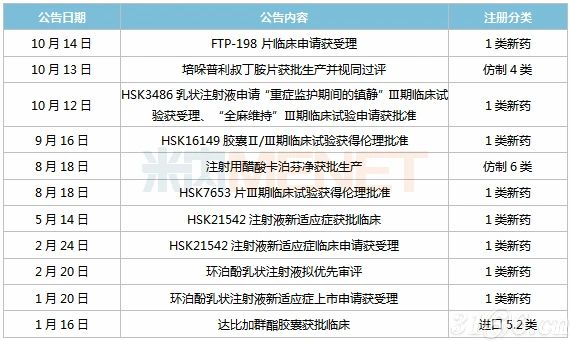
来源:上市公司公告
2020年至今,海思科有2款仿制药获批上市,分别为培哚普利叔丁胺片及注射用醋酸卡泊芬净,培哚普利叔丁胺片是一款血管紧张素转换酶(ACE)抑制剂,海思科拿下国产第2家,同时首家过评;注射用醋酸卡泊芬净是一款抗真菌药,在2019年中国公立医疗机构终端市场规模超过20亿元,在全身用抗真菌药TOP10产品中,以21.49%的市场份额排位第二。
海思科自主研发的多个1类新药有新进展,环泊酚乳状注射液(HSK3486乳状注射液)“全身麻醉诱导”适应症报产,“全麻维持”的Ⅲ期临床试验申请获得批准,申请“重症监护期间的镇静”的III期临床试验;HSK21542注射液新适应症(瘙痒症)申请临床并获批临床;HSK7653片Ⅲ期临床试验获得伦理批准;HSK16149胶囊II/III期临床试验获得伦理批准;FTP-198片临床申请获得受理。
两大爆品独家过评,10个新品在路上
10月13日,海思科发布公告称,公司以仿制4类申报的培哚普利叔丁胺片获批生产并视同过评,为国内首家。培哚普利叔丁胺是施维雅研发的一款血管紧张素转换酶(ACE)抑制剂,用于治疗高血压与充血性心力衰竭。
表2:海思科已过评品种
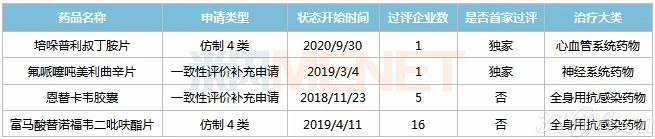
来源:米内网MED2.0中国药品审评数据库
米内网数据显示,目前海思科有4个品种通过或视同通过一致性评价,其中培哚普利叔丁胺片、氟哌噻吨美利曲辛片为独家过评,这2个品种在2019年中国公立医疗机构及城市零售药店终端合计销售规模分别超过9亿元、12亿元,且市场均由原研厂家主导,海思科的产品独家过评,有望加速仿制替代原研的进程。
表3:海思科在审的一致性评价品种(含新分类报产)
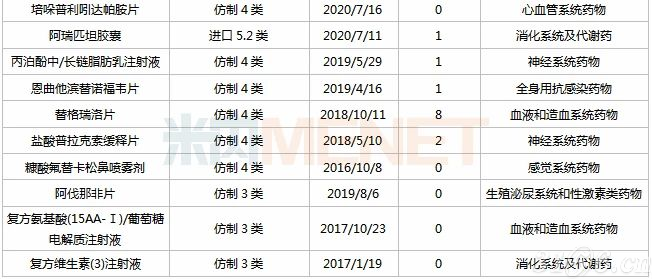

来源:米内网MED2.0中国药品审评数据库
目前海思科有9个一致性评价补充申请品种在审,均为注射剂,且均未有企业过评,其中注射用盐酸头孢替安、注射用头孢美唑钠、注射用艾司奥美拉唑钠、注射用甲泼尼龙琥珀酸钠、脂肪乳氨基酸(17)葡萄糖(11%)注射液5个品种在2019年中国公立医疗机构终端的销售规模超过10亿元。
10个新分类报产品种在审,其中阿伐那非片、复方氨基酸(15AA-I)/葡萄糖电解质注射液国内市场暂时空白,培哚普利吲达帕胺片、糠酸氟替卡松鼻喷雾剂目前仅原研产品在售。培哚普利吲达帕胺片、阿伐那非片、糠酸氟替卡松鼻喷雾剂3个品种,海思科有望以首仿+首家过评的方式获批上市。
除了注射剂及口服常释剂型,海思科还重点布局缓控释制剂及吸入剂等具有技术难度及壁垒的制剂。在缓控释制剂方面,盐酸普拉克索缓释片已按仿制4类报产,此外还引入莹硕生技的帕利哌酮缓释片、盐酸坦索罗辛口崩缓释片(未有首仿)及硝苯地平控释片等优秀外部项目;在吸入剂方面,糠酸氟替卡松鼻喷雾剂已按仿制4类报产,马来酸茚达特罗格隆溴铵粉吸入剂、格隆溴铵粉吸入剂获批临床,此外还引进了益得生技的复方布地奈德福莫特罗气雾剂(国内市场空白)等。
13款创新药在研,首个1类新药获批在即
10月12日,海思科发布公告称,公司自主研发的1类新药HSK3486乳状注射液“全麻维持”适应症获准开展III期临床,“重症监护期间的镇静”III期临床试验申请获受理;9月26日,海思科1类新药FTP-198片临床申请获得CDE承办受理。
在创新药研究领域,海思科通过建设小分子创新药研发平台,在特定细分领域针对特定靶点开发具有国际竞争力的创新药,聚焦于麻醉及镇痛、糖尿病及并发症、抗肿瘤、神经痛及呼吸系统等领域。
目前海思科处于研发阶段的创新药有13个,其中已开展临床试验的创新药有6个,HSK3486乳状注射液进展最快,已有2个适应症申报上市,第3个适应症完成III期临床;HC-1119软胶囊、HSK7653片正在进行III期临床。
表4:海思科部分在研新药
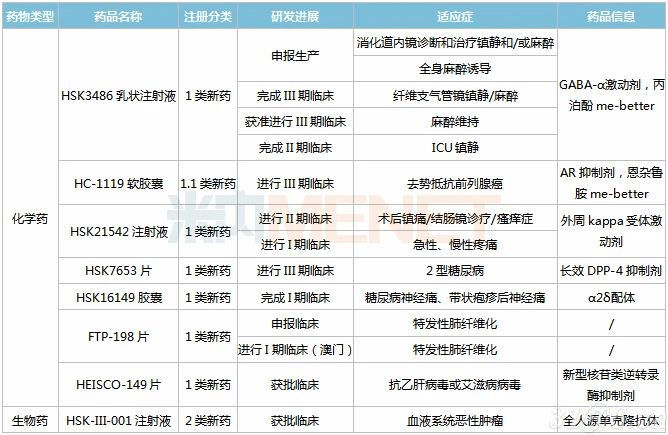
来源:米内网中国药品临床试验公示库
GABA-α激动剂HSK3486乳状注射液各项适应症稳步推进:两个适应症已申报上市,且均已递交发补材料,有望在2020年下半年获批。纤维支气管镜镇静/麻醉适应症已完成III期临床,麻醉维持适应症获准开展III期临床,ICU镇静适应症完成II期临床,目前已申请开展III期临床。
2个1类新药正在开展III期临床:雄激素受体(AR)抑制剂HC-1119软胶囊为恩杂鲁胺me-better,恩杂鲁胺是由安斯泰来/辉瑞联合开发的前列腺癌大品种,2019年全球销售额超过45亿美元(汇率以10月20日计);HSK7653片为长效DPP-4抑制剂,目前国内已获批上市的DPP-4抑制剂有5款,分别为西格列汀、沙格列汀、维格列汀、利格列汀和阿格列汀。
本文来源于网络,版权归作者所有,如有侵权请联系网站客服。
相关新闻
-
3·15后 药店检查来袭
3.15过后,药店开始面临最严检查,涉及10个重点,包括四类药销售、网络售药、过期药销售、非法进货等。【查看详情】
2022-03-16分享
-

-
中药配方颗粒开始挂网!按销售价70%纳入医保支付
3月14日,福建省医疗保障局发布《关于做好中药配方颗粒医保管理的通知》,将加强采购管理,该通知自2022年4月1日起施行。【查看详情】
2022-03-16分享
-

-
全国首次!中药饮片集采来了 千亿市场或洗牌
2022-03-09分享
-

-
集采后 430个大品种受热捧
随着带量采购不断加码乃至“双通道”政策的实施,处方药发展空间被大幅压缩,反观OTC药品,受到各项政策的影响较小,不少畅销OTC品牌更是成为了稀缺资源,受到热捧。【查看详情】
2022-03-09分享
-

-
202个大品种已满足国采条件(附名单)
近日,上海阳光医药采购网发布最新消息,第六批国采(胰岛素专项)中选结果将于2022年5月底实施。【查看详情】
2022-01-10分享

































